化学変化と質量に関する問題です。
計算問題が多く出題されます。比の計算も必要となりますので、しっかり練習するようにしてください。
質量保存の法則
化学変化の前後で、変化に関係した物質の質量は変わりません。
下の図のように うすい硫酸とうすい塩化バリウム水溶液を混ぜると硫酸バリウムという白い沈殿物ができます。
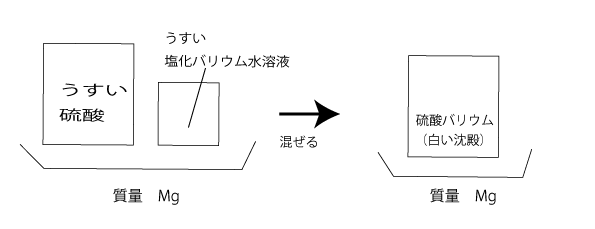
硫酸と塩化バリウム水溶液の質量と反応で出来た硫酸バリウムの質量は同じになります。
気体が発生する場合
気体が発生する化学変化では、反応後の質量は小さくなります。これは発生した気体が空気中に逃げ出すからです。
密閉した容器の中で反応させれば、化学変化の前後で質量は変わりません。
下の図のように炭酸ナトリウムに薄い塩酸を混ぜると 二酸化炭素、水、塩化ナトリウムができます。
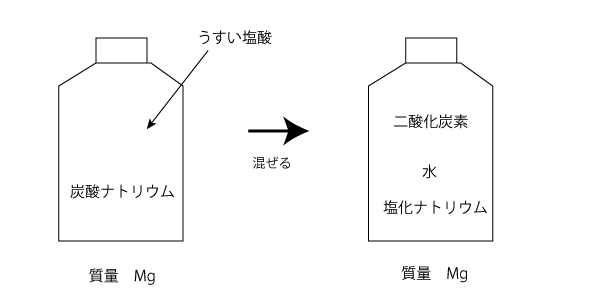
密閉した容器内では反応の前後では質量は変わりません。
フタを開けると二酸化炭素が空気中に逃げ出すので、反応前より質量は減ります。
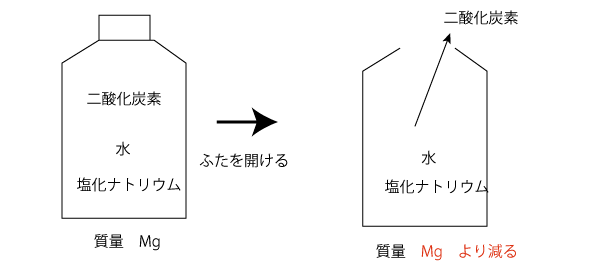
質量保存の法則が成り立つ理由
化学変化の前後では、原子の結びつき方が変わるが、原子の種類と数は変わらない。
銅と酸素を化合して酸化銅を作る反応式のモデルでは

原子の結びつきは変わっても、反応前後で原子の種類と数は変わりません。
同じ原子の質量は一定なので反応前後で質量保存の法則が成り立ちます。
定比例の法則
物質を構成する原子の質量の比は、物質の種類によって一定である。
酸化マグネシウムでは、マグネシウムと酸素の質量比は 3:2
酸化銅では、銅と酸素の質量比は 4:1
定比例の法則が成り立つ理由
銅と酸素を化合して酸化銅が出来る反応を考えます。
炭素原子1個の質量を12とすると、銅原子の質量は64、酸素原子の質量は16となります。(高校の化学で学習します。)
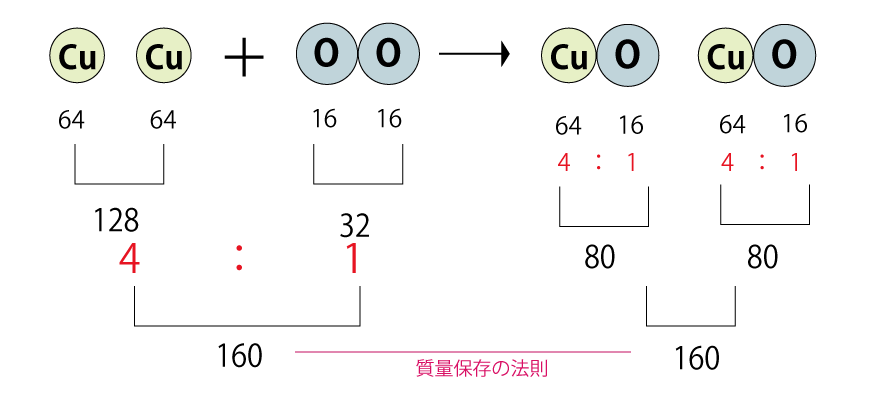
上のように銅:酸素=64:16=4:1になります。
問題例)
銅2.0を空気中で熱したら酸化銅が2.5gできた。銅8.0gを熱したら酸化銅は何gできるか。
銅:酸化銅 = 2.0 :2.5 =4:5
求める酸化銅の質量をxとすると
8.0:x =4:5 x=10.0 答 10.0g
*比の計算の復習をしておきましょう。
練習問題をダウンロードする
画像をクリックするとPDFファイルをダウンロードできます。
基本的な問題から順番にアップしています。応用問題まで作成する予定ですのでしばらくお待ちください。

