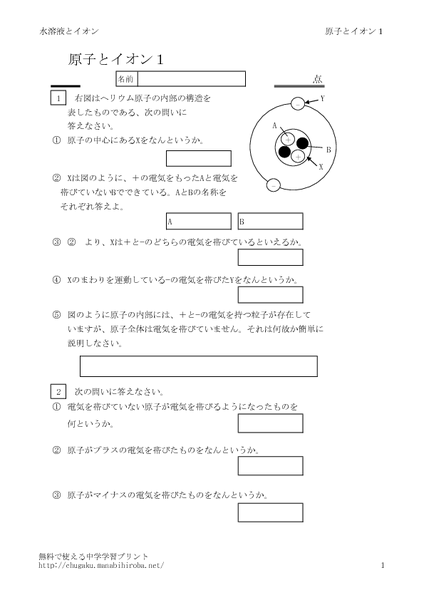
原子とイオンの基本的な問題です。
教科書で基本的な内容をしっかり理解してから、問題に取り組みましょう。
学習のポイント
- 原子の構造(原子核・陽子・中性子・電子)を理解しましょう。
- 陽イオン・陰イオンのでき方を説明できるようにしましょう。
- 代表的なイオンの化学式を覚えましょう。
- イオンの電子の数を計算できるようにしましょう。
基本事項
原子の構造
物質を構成する最小の粒子が原子です。原子は原子核と電子からできています。
原子核は原子の中心にあり、+の電気を帯びた陽子と、電気を帯びていない中性子からできています。原子核のまわりには**-の電気を帯びた電子**が運動しています。
陽子(+)の数と電子(-)の数は同じなので、原子全体としては電気を帯びていません。
| 粒子 | 電気 | 場所 |
|---|---|---|
| 陽子 | + | 原子核の中 |
| 中性子 | なし | 原子核の中 |
| 電子 | − | 原子核のまわり |
同位体
同じ元素で中性子の数が異なる原子を互いに同位体といいます。
例えば、通常の水素は中性子をもちませんが、中性子を1個もつ重水素があります。同位体どうしの化学的な性質はほとんど等しくなります。
電子配置
原子はその種類によって、電子がどの層に何個ずつ入るか決まっています。これを電子配置といいます。
- 一番内側の軌道:最大2個
- 2番目以降の軌道:それぞれ最大8個
例えばナトリウム(陽子11個、電子11個)の場合:2個+8個+1個=11個
イオンとは
原子が電子を失ったり受けとったりして、電気を帯びたものをイオンといいます。
陽イオン:原子が電子を失って、+の電気を帯びたイオン
陰イオン:原子が電子を受けとって、−の電気を帯びたイオン
例えば、ナトリウム原子は一番外側の電子1個を失ってナトリウムイオン(Na⁺)になります。塩素原子は電子1個を受けとって塩化物イオン(Cl⁻)になります。
代表的なイオンの化学式
陽イオン
| H⁺ | Na⁺ | K⁺ | Cu²⁺ | Zn²⁺ | Mg²⁺ | Ca²⁺ | Ag⁺ | Ba²⁺ | NH₄⁺ |
|---|---|---|---|---|---|---|---|---|---|
| 水素イオン | ナトリウムイオン | カリウムイオン | 銅イオン | 亜鉛イオン | マグネシウムイオン | カルシウムイオン | 銀イオン | バリウムイオン | アンモニウムイオン |
陰イオン
| Cl⁻ | OH⁻ | SO₄²⁻ | NO₃⁻ | CO₃²⁻ | S²⁻ |
|---|---|---|---|---|---|
| 塩化物イオン | 水酸化物イオン | 硫酸イオン | 硝酸イオン | 炭酸イオン | 硫化物イオン |
NH₄⁺のように異なる種類の原子が2個以上集まったイオンを多原子イオンといいます。
イオンの電子の数の求め方
原子では陽子の数=電子の数です。イオンになるとき電子が増減するので、次のように計算します。
- 陽イオン:電子の数=陽子の数-失った電子の数
- 陰イオン:電子の数=陽子の数+受けとった電子の数
例)銅イオン(Cu²⁺):銅原子の陽子は29個 → 29-2=27個
例)塩化物イオン(Cl⁻):塩素原子の陽子は17個 → 17+1=18個
中3の理科の学習におすすめ
中3理科をひとつひとつわかりやすく。改訂版 (中学ひとつひとつわかりやすく) 新品価格 |  |
理科の基本事項をしっかり学ぶのにおすすめです
練習問題をダウンロードする
画像をクリックするとPDFファイルをダウンロードできます。
その他の水溶液とイオンの問題
イオン
化学変化と電池エネルギー
- 化学電池
- 燃料電池など