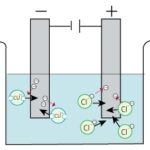
塩酸の電気分解
塩化水素を水にとかすと塩酸という水溶液になります。
塩化水素の化学式は HCl だから、電離の式は
HCl→H++Cl–
水素イオンと塩化物イオンが1:1で電離します。
電極に電圧をかける

陽極(+極)には塩化物イオン(Cl–)、陰極(-極)には水素イオン(H+)が引きよせられます。
陽極での反応
塩化物イオン(Cl–)が電子を陽極にあたえて塩素原子(Cl)になる。

*電子は動線を通って陰極に移動
陰極での反応
水素イオン(H+)が電子を陰極から受けとって水素原子(H)になる。

陽極での変化
塩素原子(Cl)が2個結びついて塩素分子(Cl2 )になり、気体の塩素として発生します。
陰極での変化
水素原子(H)が2個結びついて水素分子(H2 )になり、気体の水素として発生します。
分解でできた分子の数
塩化水素が水素と塩素に分解される化学反応式は次のようになります。
2HCl → H2 + Cl2 (出来る気体の量は1:1)
実際は塩素は水にとけてしまうので、気体を集めると水素のほうが多くなります。
練習問題をダウンロード
*画像をクリックするとPDFファイルをダウンロード出来ます。
*問題は追加する予定です。しばらくお待ち下さい。
|
新品価格 |
 |
![]()