溶液の濃度の問題です。
計算問題がメインになるので、苦手にする人も多いですが、小学校の算数がわかっていれば難しいものではありません。
基本的な用語を確認して、実際に計算問題を解いてみてください。
質量パーセント濃度の求め方
中学で学習するのは質量パーセント濃度を求めることです。
濃度とは溶液の中に溶けている溶質の割合を求めることです。→割合をパーセントで表ます。小学校の割合を%で表すあたりで自信がない場合は小学校の割合の問題を復習しましょう。
溶液や溶質の単位は質量(g)で表しますので、質量パーセントということです。
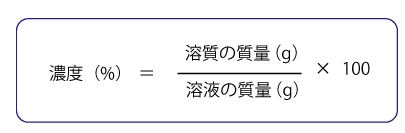
溶液の質量=溶媒の質量+溶質の質量
になることに注意してください。
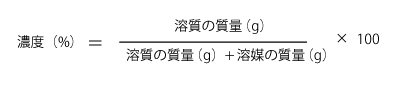
食塩水の例で具体的に図にして考えると分かりやすくなります。
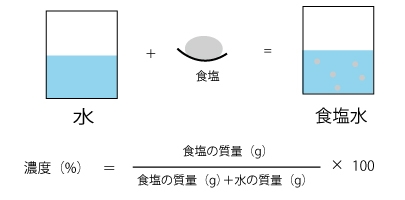
120g(食塩の水溶液の質量)=20g(食塩の質量)+100g(水の質量)
基本的な計算問題の解き方
次のような問題が基本問題として出題されます
水114gに食塩を6gとかしたとき、何%の食塩水が何gできるか
食塩水の質量=114+6=120
濃度=6÷120×100=50(%)
割合の考え方で溶質、水溶液の量を求めることができる
小学校の割合の考え方では 割合=濃度 もとになる量=溶液 くらべる量=溶質
となります。食塩水の濃度で具体的に考えると
食塩水の濃度(割合)=食塩(くらべる量)÷食塩水(もとになる量) という式です。(割合を求めから%に直せばいい)
くらべる量=もとになる量×割合
もとになる量=くらべる量÷割合
という小学校で習った式を使うことができます。
(1次方程式を習ったら、方程式を使って解いてもOKです。)
例)20%の食塩水150gには何gの食塩が溶けているか
20%→0.2 食塩(くらべる量)=食塩水(もとになる量)×割合
150×0.2=30(g)
例)15gの食塩を水に溶かして濃度が5%の食塩水を作りたい。食塩水の量と必要な水の量をもとめなさい。
5%→0.05 食塩水(もとになる量)=食塩(くらべる量)÷割合
15÷0.05=300(g)←食塩水の量
300-15=285(g) ←必要な水の量
一次方程式を習ったら応用問題が解きやすくなる
数学で1次方程式を学習したら次のような応用問題が解けるようになります。
水230gを全て使って濃度8%の食塩水の水溶液を作るために必要な食塩の質量を求めなさい。
食塩の質量をxとする
\(\frac { x }{ 230+x } \times 100=8\) \(100x=8(230+x)\\ 100x=1840+8x\\ 92x=1840\\ \quad \quad x=20\)答え 20g
一次方程式の応用問題で練習しましょう。
練習問題をダウンロード
画像をクリックするとPDFファイルをダウンロードできます。
*問題は追加する予定ですのでしばらくお待ちください。
