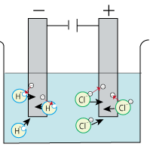
塩化銅の電気分解
塩化銅水溶液に電流を流して電気分解します。
塩化銅の電離式は次のようになります。

CuCl2→Cu2++2Cl–
銅イオンと塩化物イオンが1:2で電離します。
電極に電圧をかける

陽極(+極)には塩化物イオン(Cl–)、陰極(-極)には銅イオン(Cu2+)が引きよせられます。
陽極での反応
塩化物イオン(Cl–)が電子を陽極にあたえて塩素原子(Cl)になる。

*電子は動線を通って陰極に移動
陰極での反応
銅イオン(Cu2+)が電子を2個陰極から受けとって銅原子(Cu)になる。

陽極での変化
塩素原子(Cl)が2個結びついて塩素分子(Cl2 )になり、気体の塩素として発生します。
陰極での変化
銅原子(Cu)が陰極に銅として付着します。
*銅は赤色 軽くこすると金属光沢があらわれる。
分解の化学式
CuCl2→ Cu + Cl2 (出来る物質の量は1:1)
塩化銅水溶液は青色 (銅イオンの色)
電気分解をすすめ、水溶液中のイオンが少なくなる→電流が流れにくくなる。塩素の発生量が少なくなる。銅イオンが少なくなるので水溶液の青色が薄くなる。
練習問題をダウンロード
*画像をクリックするとPDFファイルをダウンロード出来ます。
*問題は追加する予定です。しばらくお待ち下さい。
|
新品価格 |
 |
![]()